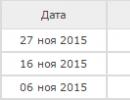
Aldehitlerin kimyasal özellikleri: gümüş ayna reaksiyonu. Gümüş ayna reaksiyonu nedir
Gümüş oksit, karmaşık bir bileşik oluşturacak şekilde çözünür - diamin gümüş(I) hidroksit OH
metalik gümüş oluşturmak için oksidasyon-indirgeme reaksiyonunun meydana geldiği bir aldehit eklendiğinde:
Reaksiyon temiz ve pürüzsüz duvarlara sahip bir kapta gerçekleştirilirse gümüş ince bir film şeklinde çökerek ayna yüzeyi oluşturur. En ufak bir kirlenme durumunda gümüş, gri, gevşek bir çökelti şeklinde salınır.
"Gümüş ayna" reaksiyonu aldehitler için kalitatif bir reaksiyon olarak kullanılabilir. Böylece “gümüş ayna” reaksiyonu glikoz ve fruktozu ayırt etmek için kullanılabilir. Glikoz bir aldozdur (açık formda bir aldehit grubu içerir) ve fruktoz bir ketozdur (açık formda bir keto grubu içerir). Bu nedenle glikoz “gümüş ayna” reaksiyonu verirken fruktoz vermez.
Edebiyat
- Nekrasov B.V. Genel kimyanın temelleri. - 3. baskı, rev. ve ek - M .: “Kimya”, 1973. - T. 2. - 688 s.
- Nesmeyanov A.N., Nesmeyanov N.A. Organik kimyanın başlangıcı. 2 cilt halinde. - 2. baskı, çev. - M .: “Kimya”, 1974. - T. 1. - 624 s.
Wikimedia Vakfı. 2010.
Diğer sözlüklerde “Gümüş Ayna Reaksiyonu”nun ne olduğunu görün:
Aynalar - Akademika'dan çalışan bir ayna alın veya Stroylandaya'da karlı bir şekilde indirime girin
Tollens reaktifi ile test edin. Solda pozitif bir test var (aldehitle reaksiyon). Sağda negatif bir test (ketonla reaksiyon) Tollens reaktifi (gümüş diamin hidroksit) gümüş amonyak OH'nin alkalin çözeltisi var. Ne zaman... ... Vikipedi
- (Latince alkol dehidrogenatum hidrojenden yoksun alkolden) bir organik bileşik sınıfı, ... Vikipedi
Ov; pl. (birim aldehit, a; m.). [çarpık enlem. hidrojen içermeyen al(kol) dehid(rogenatum) alkol]. Kimya Organik bileşikler, birincil alkollerin dehidrojenasyonunun ürünü (polimer üretiminde veya organik sentezde vb. kullanılır).... ... ansiklopedik sözlük
A. TEK İŞLEVLİ BİLEŞİKLER 1. C1: organometalik bileşikler. Bu bileşikler genellikle iki yöntemle hazırlanır: a) aktif bir metalin (Na, Li, Mg, Zn) bir organik halojenür üzerindeki etkisi ile, veya b) bir halojenürün daha az etkisi ile... .. . Collier Ansiklopedisi
Polimer- (Polimer) Polimer tanımı, polimerizasyon türleri, sentetik polimerler Polimer tanımı, polimerizasyon türleri, sentetik polimerler hakkında bilgiler İçindekiler İçindekiler Tanım Tarihsel referans Polimerizasyon Türleri Bilimi... ... Yatırımcı Ansiklopedisi
Bu makale kimyasal hakkındadır. Gıda ürünü için bkz. Şeker . Sükroz ... Vikipedi
I (kimyasal, Fransızca Gliserin, Almanca ve İngilizce gliserin) C2H3O2 = C2H5(OH)2, 1779'da Scheele tarafından keşfedildi ve kaynatma sırasında şunu fark etti: zeytin yağı Liharji ile kurşun alçıya (kurşun sabunu, yani yağ asitlerinin kurşun tuzu) ek olarak... ...
Sükroz Genel Sistematik adı a D glukopiranosil b D fruktofuranosid Kimyasal formül... Vikipedi
- (C, atom ağırlığı 12) doğada yaygın olarak dağılan elementlerden biridir. Bitki ve hayvan dokularının bir parçası olan (hidrojen, oksijen ve nitrojenle birlikte) U, tüm yaşam süreçlerinde önemli bir rol oynar... ... Ansiklopedik Sözlük F.A. Brockhaus ve I.A. Efron
Gümüş- (Gümüş) Gümüş tanımı, gümüş madenciliği, gümüşün özellikleri Gümüşün tanımı, gümüş madenciliği, gümüşün özellikleri hakkında bilgiler İçindekiler İçindekiler Tarih Keşif. Olası gümüş kıtlığı ve büyüme kelimesinden alıntı isimler Tablonun tarihi... Yatırımcı Ansiklopedisi
Her organik madde sınıfının, temsilcilerinin diğer maddelerden ayırt edilebileceği belirli bir reaksiyona sahip olduğu gerçeğiyle başlayalım. Okul kimyası dersi, organik maddelerin ana sınıfları için tüm yüksek kaliteli reaktiflerin incelenmesini içerir.
Aldehitler: yapısal özellikler
Bu sınıfın temsilcileri, radikalin bir aldehit grubuna bağlı olduğu doymuş hidrokarbonların türevleridir. Ketonlar aldehitlerin izomerleridir. Benzerlikleri, karbonil bileşikleri sınıfına ait olmalarında yatmaktadır. Bir karışımdaki aldehitin izole edilmesini içeren bir görevi gerçekleştirirken, bir "gümüş ayna" reaksiyonu gerekli olacaktır. Bu kimyasal dönüşümün özelliklerini ve uygulama koşullarını analiz edelim. Gümüş ayna reaksiyonu, gümüş metalin gümüş diamin(1) hidroksitten indirgenmesi işlemidir. Basitleştirilmiş haliyle, bu karmaşık bileşiği gümüş oksitin basitleştirilmiş biçiminde yazmak mümkündür (1).
Karbonil bileşiklerinin ayrılması
Karmaşık bir bileşik oluşturmak için gümüş oksit amonyak içinde çözülür. İşlemin geri dönüşümlü bir reaksiyon olduğu göz önüne alındığında, gümüş ayna reaksiyonu taze hazırlanmış gümüş oksit amonyak çözeltisi ile gerçekleştirilir (1). Argentumun karmaşık bir bileşiği bir aldehit ile karıştırıldığında bir redoks reaksiyonu meydana gelir. İşlemin tamamlandığı metalik gümüşün çökelmesiyle gösterilir. Etanal ve amonyak gümüş oksit çözeltisinin etkileşimi doğru bir şekilde gerçekleştirildiğinde, test tüpünün duvarlarında gümüş bir kaplama oluşumu gözlenir. Bu etkileşime “gümüş ayna” adını veren görsel efektti.

Karbonhidratların belirlenmesi
Gümüş aynanın reaksiyonu bir aldehit grubu için nitelikseldir, dolayısıyla organik kimya derslerinde glikoz gibi karbonhidratları tanımanın bir yolu olarak da bahsedilmektedir. Aldehit-alkol özelliği gösteren bu maddenin kendine özgü yapısı dikkate alındığında “gümüş ayna” reaksiyonu sayesinde glikozu fruktozdan ayırmak mümkündür.Dolayısıyla bu sadece aldehitlere karşı kalitatif bir reaksiyon değil, aynı zamanda diğer birçok organik madde sınıfını tanımanın bir yolu.

“Gümüş aynanın” pratik uygulaması
Aldehitlerin ve amonyak gümüş oksit çözeltisinin etkileşimi ile ne gibi zorluklar ortaya çıkabilir? Sadece gümüş oksit satın almanız, amonyak stoklamanız ve bir aldehit seçmeniz yeterli - ve deneye güvenle başlayabilirsiniz. Ancak bu kadar ilkel bir yaklaşım araştırmacıyı istenilen sonuca götürmeyecektir. Test tüpünün duvarlarında beklenen ayna yüzeyi yerine şunu göreceksiniz: en iyi durum senaryosu) koyu kahverengi gümüş süspansiyon.

Etkileşimin özü
Gümüşe yüksek kaliteli bir tepki, belirli bir eylem algoritmasına bağlılığı ifade eder. Çoğu zaman, bir ayna katmanının işaretleri ortaya çıktığında bile, kalitesi açıkça arzulanan çok şey bırakıyor. Böyle bir başarısızlığın nedenleri nelerdir? Onlardan kaçınmak mümkün mü? İstenmeyen sonuçlara yol açabilecek birçok sorun arasında iki ana sorun vardır:
- kimyasal etkileşim koşullarının ihlali;
- gümüşleme için zayıf yüzey hazırlığı.
Başlangıç maddelerinin çözeltideki etkileşimi sırasında gümüş katyonları oluşur, aldehit grubuyla birleşerek sonuçta koloidal küçük gümüş parçacıkları oluşturur. Bu tanecikler cama yapışabilir ancak çözelti içinde gümüş süspansiyon halinde muhafaza edilebilir. Parçacık yapışmasının gerçekleşmesi için soy metal cam ile düzgün ve dayanıklı bir tabaka oluşur, camın önceden yağdan arındırılması önemlidir. Yalnızca test tüpünün başlangıç yüzeyinin tamamen temiz olması durumunda, düzgün bir gümüş tabakanın oluşması beklenebilir.
Olası sorunlar
Cam eşyaların ana kirletici maddesi, çıkarılması gereken yağlı kalıntılardır. Alkali bir çözeltinin yanı sıra sıcak krom karışımı da sorunun çözülmesine yardımcı olacaktır. Daha sonra test tüpü damıtılmış su ile yıkanır. Alkali yoksa sentetik bulaşık deterjanı kullanabilirsiniz. Yağdan arındırma işlemi tamamlandıktan sonra cam kalay klorür çözeltisi ile yıkanır ve su ile durulanır. Çözeltilerin hazırlanmasında damıtılmış su kullanılır. Eğer mevcut değilse yağmur suyunu kullanabilirsiniz. Glikoz ve formaldehit, saf bir maddenin bir çözeltiden çökelmesine izin veren indirgeyici maddeler olarak kullanılır. Aldehit ile yüksek kaliteli bir gümüş kaplama elde edileceğine güvenmek zordur, ancak bir monosakarit (glikoz) aynanın yüzeyinde düzgün ve dayanıklı bir gümüş tabaka sağlar.

Çözüm
Gümüş cam için gümüş nitrat kullanılması tavsiye edilir. Bu tuzun çözeltisine alkali ve amonyak çözeltisi eklenir. Tam bir reaksiyonun ve gümüşün cam üzerinde birikmesinin koşulu, alkali bir ortamın yaratılmasıdır. Ancak bu reaktifte fazlalık varsa, yan etkiler. Seçilen deneysel tekniğe bağlı olarak ısıtma yoluyla yüksek kaliteli bir reaksiyon elde edilir. Çözümün renklendirilmesi kahverengi renk küçük koloidal gümüş parçacıklarının oluşumunu gösterir. Daha sonra camın yüzeyinde bir ayna kaplama belirir. İşlem başarılı olursa metal katman pürüzsüz ve dayanıklı olacaktır.
Seçmeli ders “Organik Kimya Deneyi” dersinin yürütülmesi
Ders araştırması
Pratik çalışma No. 3 “Gümüş ayna reaksiyonu”
Ders: Çeşitli sınıflara ait organik bileşiklerin gümüş (I) bileşikleri ile etkileşimlerinin incelenmesi.
Dersin amacı:
Genel Eğitim
Organik bileşik sınıflarının gümüş bileşiklerle etkileşimini araştırın, bu etkileşimin seçiciliğinin nedenini bulun.
Gelişimsel
Düşünme becerilerinin geliştirilmesi, karşılaştırma, analiz, bilişsel becerilerin sentezi. Soru sorma ve sorma, problemi formüle etme ve sonuç çıkarma becerisi; bağımsız davranış becerilerini geliştirmek.
Didaktik
Bağımsız alanda yetkinlikleri geliştirmek bilişsel aktivite, takım çalışması becerileri, bir sorunu görme ve onu çözmenin yollarını özetleme yeteneği.
eğitici
İdeolojik düşüncenin oluşması, ufukların genişlemesi, konunun incelenmesine yönelik olumlu bir tutumun oluşması, yoldaşlara yardım etme alışkanlığı, gerçekleştirilen göreve karşı vicdanlı bir tutum, kendine ve yoldaşlara yönelik taleplerin geliştirilmesi.
Yöntemler: araştırmak, çalışmak eğitim literatürü, kısmen arama, laboratuvar çalışması, grup.
Teçhizat: Öğrenci masalarında “Gümüş Ayna” Reaksiyonu” laboratuvar çalışmasının yapılmasına yönelik alet ve reaktifler, görev kartları ve derse yönelik bir sunum bulunmaktadır.
Dersler sırasında
“Mucizelerin zamanı geçti ve biz
Nedenlerini aramalısın
Dünyada olup biten her şey"
W. Shakespeare
(1 numaralı slayt)
Öğretmenin açılış konuşması : Kimya bilimi hakkında fikri olan herkes, kimyasal deneyin ayrılmaz bir parçası olduğunu bilir. Eğlenceli deneyler Ve pratik dersler Kimyasal düşüncenin geliştirilmesine ve kimyanın asimilasyonunun teşvik edilmesine yardımcı olun. Seçmeli ders “Deneysel problemler sistemi aracılığıyla organik kimyanın incelenmesi” 17 saat 12 pratik çalışma için tasarlanmıştır. Pratik çalışmaların çoğu küçük öğrenci gruplarında gerçekleştirilir. Ders çalışması aşağıdaki şekilde yapılandırılmıştır. Öğrenciler yaklaşan pratik çalışmanın konusuyla ilgili ödevler alırlar. Evde teorik materyalle tanışırlar ve işin içeriğini incelerler.
Bugün tutuyoruz pratik iş 3 numara (yukarıdaki başlığa bakın)
(2 numaralı slayt)
Bu çalışmanın amacı: Organik bileşik sınıflarının gümüş bileşiklerle etkileşimini deneysel olarak incelemek, bu etkileşimin seçiciliğinin nedenini bulmak, deneycinin faaliyetlerinde gerekli pratik becerileri pekiştirmek.
(3 numaralı slayt)
Öğrenciler ders için ön ödev aldılar.
Öğretmen : Gümüş bileşiğinin reaksiyonuna “gümüş ayna reaksiyonu” denir. Bize bu aynayı nasıl aldığınızın hikayesini anlatın.
1 öğrenci : Aynayı almanın hikayesi. Aynalar... BuBu hayatımızda tamamen gündelik bir şey. Çok az insan aynaların çağımızdan çok önce ortaya çıktığını biliyor. İlk başta bunlar altın, gümüş, bakır veya bronzdan yapılmış, parlatılan metal plakalardı. Modern aynaların (cam üzerine) üretimine 1858 yılında Alman kimyager Justus Liebig tarafından başlandı. Bu amaçla gümüş katyonlarının çok sayıda karmaşık bileşik oluşturma yeteneğinden yararlandı.Bir gün, şişenin iç yüzeyini bir soda çözeltisiyle ve ardından su, etil alkol ve dietil eterle yıkadıktan sonra Liebig, içine biraz seyreltilmiş formaldehit -% 10'luk bir formaldehit çözeltisi - döktü. Daha sonra formaldehite gümüş amonyak bileşiğinden oluşan bir çözelti ekleyerek şişeyi dikkatlice ısıttı.Birkaç dakika sonra şişe aynaya benzedi.
Gümüş içeren kompleks katyon metale (gümüş) indirgenir ve formaldehit formik asit HCOOH'ye oksitlenir. Daha sonra Justus Liebig formaldehit yerine glikoz kullanarak “gümüş ayna”yı elde etti.
Öğretmen : Analitik kimyada yaygın olarak kullanılan Tollens reaktifinin üretim tarihini anlatın.
2 öğrenci: Tollens reaktifinin elde edilmesinin tarihi. 1881'de Alman kimyager Bernhard Christian Tollens, çözeltide aldehit grubu bulunan bileşikleri tespit etmek için gümüş kompleksi bileşiğinin kullanılmasını önerdi. Bir gümüş nitrat çözeltisine sulu bir amonyak çözeltisi eklendiğinde, normal koşullar altında gümüş hidroksit mevcut olmadığından gri-siyah bir oksit çökeltisi çöker.
2AgNO3 + 2NH4OH → Ag2O + 2NH4NO3 + H2O
Gümüş oksit amonyak fazlası suda çözünür ve bir kompleks oluşturur birlik.
Ag 2 O + 4NH4 OH → 2 OH +3H 2 O
Ortaya çıkan renksiz çözeltiye Tollens reaktifi denir.
2. Ana bölüm
“Kimyager olmanın yolu yok,
Uygulamanın kendisini görmeden
ve kimyasal işlemlere başlamadan"
M.V. Lomonosov
(4 numaralı slayt)
A) Rol yapma oyunu: Sınıf, çeşitli sınıflardaki organik bileşiklerin gümüş (I) bileşikleri ile etkileşimlerini incelemek üzere çalışmalarına başlayan bir araştırma laboratuvarıdır. Öğrenciler üç yaratıcı gruba ayrılır. Her yaratıcı grubun bir bilgi departmanı ve bir kimya laboratuvarı vardır. Gruplara teorik ve pratik görevler verilir ve çalışmalar yapılır (5-7 dakika). Görevle birlikte deneyin tamamlanmasına yönelik talimatlar da verilmektedir. (5 numaralı slayt)
Görev 1 yaratıcı grubu
Görev 2 yaratıcı grubu
Etkileşime giriyor mu? Neden?
Bilgilendirme Departmanı: Yayımlanan maddeler hangi organik bileşik sınıflarına aittir? Hangi fonksiyonel gruplara sahipler?
Görev 3 yaratıcı grubu
Bilgilendirme Departmanı: Yayımlanan maddeler hangi organik bileşik sınıflarına aittir? Hangi fonksiyonel gruplara sahipler?
(6 numaralı slayt)
"Düşünen zihin kendini mutlu hissetmez,
Farklı gerçekleri birbirine bağlamak mümkün olana kadar,
onun tarafından gözlemlendi"
D. Hevesy.
(7 numaralı slayt)
B) Her grubun raporlarının tartışılması
Öğretmen : Ve şimdi yaratıcı grupların yapılan çalışmalar hakkında rapor vermesi gerekiyor. Kimya laboratuvarındaki bir öğrenci, deney sırasında meydana gelen gözlemlerini anlatıyor ve gümüş bileşiğinin etkileşime girdiği sınıf hakkında bir sonuca varıyor. Bu sırada bilgi bölümünü oluşturan öğrenci dışarı çıkar ve organik bir maddenin gümüş (I) oksit ile etkileşimi için reaksiyon denklemini her sınıfın fonksiyonel grubunu vurgulayarak yazar.
Reaksiyon kaydı ilgili 8, 9,10 numaralı slaytta kontrol edilir.
Genel sonuç, Tollens reaktifinin (gümüş bileşiği (I)) aldehitler, glikoz ve formik asitte bulunan aldehit grubu için kalitatif olduğu şeklinde formüle edilmiştir. (11 numaralı slayt)
Ders özetlenmiştir.
"Görmenin ve anlamanın sevinci
en güzel hediye var"
A.Einstein
(12 numaralı slayt)
Gümüş ayna reaksiyonu aynalar, gümüş kaplama dekorasyonlar ve Noel ağacı süsleri yapmak için kullanılır.
Maddelerin kalitatif analizi organik kimya çalışmalarında önemli bir konudur. Bunun bilgisi sadece kimyagerlere değil, aynı zamanda doktorlara, ekolojistlere, biyologlara, epidemiyologlara, eczacılara ve gıda endüstrisi çalışanlarına da çalışmalarında yardımcı olur.
Çözüm. Sonuçları özetliyoruz ve derecelendirmeler veriyoruz. İlginiz için teşekkür ederiz!
Laboratuvar deneyi için talimatlar
“Gümüş ayna” reaksiyonu
Bir test tüpüne 2 ml %1'lik gümüş nitrat AgNO3 çözeltisi dökün ve elde edilen gümüş oksit çökeltisi tamamen eriyene kadar küçük porsiyonlar halinde %10 amonyak suyu NH4OH ekleyin. (Veya hazır Tollens reaktifini kullanın)
Elde edilen çözeltiye 1 ml ekleyin. deney maddesi. Test tüpünü alevin etrafında döndürerek, alt kısım yerine duvarları ısıtarak içindekileri ısıtın. Test tüpünü dik tutun.
1. Test tüpünde ne gözlemliyorsunuz?
2. Cam yüzeyi neden aynaya benziyor?
3. Reaksiyonun denklemini yazın.
Laboratuvar deneyi için talimatlar
“Gümüş ayna” reaksiyonu
Bir test tüpüne 2 ml %1'lik gümüş nitrat AgNO3 çözeltisi dökün ve elde edilen gümüş oksit çökeltisi tamamen eriyene kadar küçük porsiyonlar halinde %10 amonyak suyu NH4OH ekleyin. (Veya hazır Tollens reaktifini kullanın)
Elde edilen çözeltiye 1 ml ekleyin. deney maddesi. Test tüpünü alevin etrafında döndürerek, alt kısım yerine duvarları ısıtarak içindekileri ısıtın. Test tüpünü dik tutun.
1. Test tüpünde ne gözlemliyorsunuz?
2. Cam yüzeyi neden aynaya benziyor?
3. Reaksiyonun denklemini yazın.
Laboratuvar deneyi için talimatlar
“Gümüş ayna” reaksiyonu
Bir test tüpüne 2 ml %1'lik gümüş nitrat AgNO3 çözeltisi dökün ve elde edilen gümüş oksit çökeltisi tamamen eriyene kadar küçük porsiyonlar halinde %10 amonyak suyu NH4OH ekleyin. (Veya hazır Tollens reaktifini kullanın)
Elde edilen çözeltiye 1 ml ekleyin. deney maddesi. Test tüpünü alevin etrafında döndürerek, alt kısım yerine duvarları ısıtarak içindekileri ısıtın. Test tüpünü dik tutun.
1. Test tüpünde ne gözlemliyorsunuz?
2. Cam yüzeyi neden aynaya benziyor?
3. Reaksiyonun denklemini yazın.
Görev 1 yaratıcı grubu
Kimya laboratuvarı: Test tüpleri iki organik madde içerir: glikoz ve etanol.Bu maddelerin reaksiyonunu gümüş (I) oksitin amonyak çözeltisiyle gerçekleştirin. Hangi madde etkileşime girmez? Neden?
Bilgilendirme Departmanı: Yayımlanan maddeler hangi organik bileşik sınıflarına aittir? Hangi fonksiyonel gruplara sahipler?
Görev 2 yaratıcı grubu
Kimya laboratuvarı: Test tüpleri iki organik madde içerir: formaldehit (formalin, metanal) ve asetik asit, bu maddelerin gümüş (I) oksitin amonyak çözeltisi ile reaksiyonunu gerçekleştirir. maddelerden hangisi değildir etkileşime giriyor mu? Neden?
Bilgilendirme Departmanı: Yayımlanan maddeler hangi organik bileşik sınıflarına aittir? Hangi fonksiyonel gruplara sahipler?
Görev 3 yaratıcı grubu
Kimya laboratuvarı: Test tüplerinde iki organik madde vardır: formik asit ve gliserol, bu maddelerin gümüş (I) oksitin amonyak çözeltisi ile reaksiyonunu gerçekleştirir. Hangi madde etkileşime girmez? Neden?
Bilgilendirme Departmanı: Yayımlanan maddeler hangi organik bileşik sınıflarına aittir? Hangi fonksiyonel gruplara sahipler?
"Gümüş ayna" reaksiyonu, gümüş oksitin (Tollens reaktifi) amonyak çözeltisi içinde gümüşün indirgenme reaksiyonudur. Sulu bir amonyak çözeltisinde gümüş oksit, karmaşık bir bileşik oluşturur - gümüş diamin hidroksit OH
Ag 2 O + 4 NH4 OH => 2 OH + H 2 O
bir aldehite maruz bırakıldığında, bir amonyum tuzunun oluşmasıyla bir redoks reaksiyonu meydana gelir:
R-CH=O + 2 OH => RCOONH 4 + 2 Ag +3 NH3 + H2O
Gümüş ayna, çok konsantre olmayan çözeltilerden bir kabın pürüzsüz duvarlarında indirgenmiş gümüş biriktirildiğinde oluşur. En ufak yabancı maddeler, indirgenmiş gümüşün cama "yapışmasını" engeller ve gevşek bir çökelti olarak çökelmesine neden olur.
Ketonların oksitlenmesi aldehitlere göre çok daha zordur, bu nedenle ketonlar "gümüş ayna" reaksiyonu vermez, dolayısıyla "gümüş ayna" reaksiyonu aldehitler için kalitatif bir reaksiyon olarak kullanılabilir. Böylece “gümüş ayna” reaksiyonu glikoz ve fruktozu ayırt etmek için kullanılabilir. Glikoz bir aldozdur (açık formda bir aldehit grubu içerir) ve fruktoz bir ketozdur (açık formda bir keto grubu içerir). Bu nedenle glikoz “gümüş ayna” reaksiyonu verirken fruktoz vermez.
HOCH2 (CHOH) 4 HC=O + 2 OH => HOCH 2 (CHOH) 4 COOH + 2 Ag +3 NH3 + H20
42. Disakkaritler. İndirgeyici ve indirgeyici olmayan disakkaritler. Sakaroz. Maltoz. Selüloz. Laktoz Disakkaritler
Disakkaritler, mineral asitlerin varlığında veya enzimlerin etkisi altında suyla ısıtıldığında hidrolize uğrayarak iki monosakkarit molekülüne bölünen karbonhidratlardır.
En yaygın disakkarit sakaroz(kamış veya pancar şekeri). Şeker kamışından veya şeker pancarından elde edilir. Sütte %5 oranında laktoz – süt şekeri bulunur. MaltozÇimlenmekte olan tahıllarda bulunur ve tahıl nişastasının hidrolizi sırasında oluşur. Selobiyoz Selülozun enzimatik hidrolizinde bir ara üründür.
Yapı. Bir disakkarit molekülü, bir glikosidik bağ ile birbirine bağlanan iki monosakkarit molekülünden oluşur. Glikozidik bağın oluşumunda hangi karbon atomlarının yer aldığına bağlı olarak disakarit molekülü, serbest bir karbonil grubu içerebilir veya içermeyebilir.
Disakkaritler ikiye ayrılabilir iki grup: onarıcı olmayan ve onarıcı. İndirgeyici olmayan şekerlerin herhangi bir anomerik merkezde bir OH grubu yoktur, indirgeyici şekerlerin ise anomerik merkezde serbest bir OH grubu vardır.
İndirgeyici olmayan şekerlere glikozil glikozitler denir; azaltıcı - glikosil-glikozlar.
Maltoz Nişastanın enzimatik hidrolizi sırasında oluşan indirgeyici bir disakkarit. Maltoz, pozisyonlarda bir glikosidik bağ ile bağlanan iki D-glikoz kalıntısından oluşur.
Sakaroz 1,2-glikosidik bağ ile bağlanan glikoz ve fruktoz kalıntılarından oluşur. Sükrozda, her iki monosakarit molekülünün hemiasetal hidroksil grupları bir glikosidik bağ oluşumuna katılır, bunun sonucunda sükroz indirgeyici olmayan bir şeker olur.
Disakkaritlerin kimyasal özellikleri:
1) hidrolize olma yeteneği: bir asitin veya uygun bir enzimin etkisi altında glikosidik bağ kırılır ve iki monosakarit oluşur;
2) bakır, gümüş, cıva iyonları ile oksitlenir, osazonlar oluşturur ve serbest karbonil grupları içeren bileşiklerin tüm karakteristik reaksiyonlarına girer;
3) disakkaritler karbondioksit ve suya oksitlenebilir. Maya enzimlerinin etkisi altında sakaroz ve maltoz etanol üretir, ancak laktoz değişmeden kalır.
Laktoz bir disakkarittir, yani minimum yapısal birimleri temsil eden iki temel şekerden oluşur. Herhangi bir kompleks karbonhidrat (örneğin nişasta, laktoz veya selüloz), kan tarafından emilen ve vücut tarafından çeşitli ihtiyaçlar için kullanılan monosakkaritlere parçalanır. Laktoz iki monosakaritten (glikoz ve galaktoz) oluştuğundan, sindirim enzimlerinin etkisi altında insan vücuduna girdiğinde tüm bileşik onlara ayrışır. Laktozun glikoz ve galaktoza parçalanmasının bir sonucu olarak galaktoz kana emilir ve insan vücudunun hücreleri tarafından kullanılır. Sindirim sisteminde laktozu galaktoz ve glikoza parçalayan enzime laktaz denir.
43.Polisakaritler. Nişasta, glikojen, lif, yüksek moleküler ağırlıklı polisakkaritler Polisakkaritler- Molekülleri onlarca, yüzlerce veya binlerce monomerden - monosakaritlerden oluşan karmaşık yüksek moleküllü karbonhidratlar sınıfının genel adı.
Polisakkaritler hayvan ve bitki organizmalarının yaşamı için gereklidir. Vücudun metabolizması sonucunda üretilen ana enerji kaynaklarından biridir. Bağışıklık süreçlerinde yer alırlar, dokularda hücre yapışmasını sağlarlar ve biyosferdeki organik maddenin büyük kısmını oluştururlar.
· nişasta bitki organizmalarında enerji rezervi olarak biriken ana polisakkarittir;
· glikojen, hayvan organizmalarının hücrelerinde enerji rezervi olarak biriken bir polisakkarittir, ancak bitki ve mantarların dokularında küçük miktarlarda bulunur;
· selüloz bitki hücre duvarlarının ana yapısal polisakkaritidir;
Nişasta (C6H10O5)n– iki fraksiyondan oluşan bir polisakkarit: %25 doğrusal amiloz ve %75 dallanmış amilopektin. Bitkilerde fotosentez sırasında ışıkta oluşur. Bu madde Beyaz toz içinde çözünmeyen soğuk su, bir süspansiyon oluşturuyor. Süspansiyon çöktükten sonra kabın dibinde beyaz bir çökelti birikir ve su kolayca boşaltılabilir. Nişasta kuruduktan sonra tüm özelliklerine kavuşur.
Sıcak suda bu madde koloidal bir çözelti oluşturur - bu, aynı zamanda nişasta macunu olarak da adlandırılan ve günlük yaşamda sıklıkla yapıştırıcı olarak kullanılan yapışkan bir sıvıdır. Jölelerin ve bazı tatlıların hazırlanışı da bu özelliğe dayanmaktadır. Nişasta kimyasal olarak inert bir maddedir. Reaksiyona girebilmesi için katalizörlerin bu sürece dahil olması gerekir. Bu maddenin kullanımı fiziksel ve kimyasal özelliklerine dayanmaktadır. Bu nedenle nişasta ve türevleri gıda, tekstil ve kağıt endüstrilerinde sıklıkla kullanılmaktadır. Ve canlı organizmalar için önemli bir rol oynar. Bu organik maddenin endüstriyel amaçlarla kullanılması için kimyasal işlemlere tabi tutulur. Nişasta hidrolizi, bir maddenin iyonları ile enzimatik veya asidik olabilen su arasındaki bir değişim işlemidir. Nişastanın kimyasal hidrolizi, inorganik asitlerin varlığında ısıtıldığında meydana geldiği için katalitik bir reaksiyondur. Bu kimyasal reaksiyon sırasında, şu denklemle ifade edilebilen glikoz oluşur: (C6H10O5)n + nH2O + (kat. H2SO4 + t°) = nC6H12O6.
Ancak son zamanlarda nişastanın enzimatik hidrolizi çok popüler hale geldi. Özel teknolojiler kullanılarak, kimyasal hidrolizle aynı şekilde etil alkol, melas ve glikoz elde edilir. Bu işlemin avantajı, başlangıç malzemesi olarak çavdar, patates, mısır, pirinç ve diğerleri gibi nişasta içeren bitkilerin alınmasıdır. Bu kaynaklar ayrıca hidroliz işleminde kullanılan amilolitik enzimleri de içerir. Örneğin bu tür enzimler izoamilaz, pullulanaz ve glikolinazdır. Enzimler kimyasal reaksiyonları hızlandıran doğal katalizörlerdir. Şematik olarak, enzimlerin etkisi altında nişastanın parçalanma süreci şuna benzer: nişasta → çözünür nişasta (amiloz) → oligosakkaritler (dekstrinler) → disakkarit (maltoz = malt) → a-glikoz. Şu denklemle de ifade edilebilir: (C6H10O5)n + nH2O + (kat. enzim) = nC6H12O6 Kimyasal hidrolizin gerçekleştiğini bir deney yaparak açıkça görebilirsiniz. Nişasta ezmesi ve sülfürik asit karışımını kaynatın. Hidrolizin meydana gelip gelmediğini kontrol ediyoruz - iyotu bırakın. Reaksiyon negatifse, yani mavi veya mor renk yoksa hidroliz meydana gelmiştir. Şimdi hidroliz ürününün glikoz olduğunu kanıtladık. Ortaya çıkan çözeltiye alkali ve bakır (II) sülfat (CuSO4) ekleyin. Bakır hidroksit çökeltisi çökelmez; çözelti parlak mavi bir renk alır. Onu ısıtıyoruz ve pişmiş toprak (tuğla) renkli bir çökelti oluşumunu görüyoruz - bu, çözeltinin hidroliz sırasında oluşan glikoz içerdiği anlamına gelir. Nişastanın enzimatik hidrolizi insan vücudunda da meydana gelir. Bu süreç çok önemlidir çünkü karbonhidratlar, özellikle de glikoz üretir. Vücudun normal işleyişi için gerekli olan enerjiyi serbest bırakırken, vücudun her hücresinde oksitlenerek su ve karbondioksit oluşturur. Nişastanın enzimler yardımıyla hidrolizi, yiyecek çiğnerken ağız boşluğunda başlar. İnsan tükürüğü, etkisi altında nişastanın daha basit bileşenlere (dekstrinler) parçalandığı bir enzim - amilaz içerir. Hatta kişi bu süreci hissedebilir. Sonuçta ekmeği uzun süre çiğnerseniz ağzınızda tatlı bir tat belirir, bu da nişasta hidroliz sürecinin başladığını gösterir. Hidroliz sırasında oluşan fazla glikoz, karaciğerde yedek besin - glikojen formunda biriktirilir.
6 45. Pektin maddeleri kavramı. Modifiye nişasta ve hemiselüloz kavramı.
Pektik maddeler, 1,4 bağlarıyla bağlanan b-D-galakturonik asit kalıntılarından oluşan karmaşık polisakkaritler - poligalakturonitlerdir.
Üç tür pektin maddesi vardır:
Protopektin - suda çözünmez bileşen hücre çeperi;
Pektin, metil ester bağları içeren galakturonik asitin suda çözünür bir polimeridir;
Pektik asit, metil ester bağları içermeyen, galakturonik asidin suda çözünebilen bir polimeridir. Pektik asit, kalsiyum tuzları ile muameleden sonra katı bir pektin jeli oluşturabilen uzun galakturonik asit zincirlerinden oluşur.
5 numaralı laboratuvar çalışması
Özelliklerkarbonhidratlar
Deney 1. Gümüş aynanın reaksiyonu bir iyileşme reaksiyonudur gümüş amonyak çözeltisinden gümüş oksit (Tollens reaktifi).
Sulu çözeltide amonyak gümüş oksit karmaşık bir bileşik oluşturacak şekilde çözünür - diamin gümüş(I) hidroksit OH
hangisine eklendiğinde aldehit metalik gümüş oluşturmak için bir redoks reaksiyonu meydana gelir:
Reaksiyon temiz ve pürüzsüz duvarlara sahip bir kapta gerçekleştirilirse gümüş ince bir film şeklinde çökerek ayna yüzeyi oluşturur.
En ufak bir kirlenme durumunda gümüş, gri, gevşek bir çökelti şeklinde salınır.
"Gümüş ayna" reaksiyonu aldehitler için kalitatif bir reaksiyon olarak kullanılabilir. Bu nedenle, “gümüş ayna” reaksiyonu, aralarında ayırt edici bir reaksiyon olarak kullanılabilir. glikoz Ve fruktoz. Glikoz bir aldozdur (açık formda bir aldehit grubu içerir) ve fruktoz bir ketozdur (açık formda bir keto grubu içerir). Bu nedenle glikoz “gümüş ayna” reaksiyonu verirken fruktoz vermez. Ancak çözeltide alkalin bir ortam mevcutsa, ketozlar aldoza izomerleşir ve ayrıca amonyak çözeltisiyle pozitif reaksiyonlar verir. gümüş oksit (Tollens reaktifi).
Glikozun amonyak gümüş oksit çözeltisi ile kalitatif reaksiyonu. Glikozda bir aldehit grubunun varlığı, gümüş oksitin amonyak çözeltisi kullanılarak kanıtlanabilir. Gümüş oksitin amonyak çözeltisine glikoz çözeltisi ekleyin ve karışımı bir su banyosunda ısıtın. Kısa süre sonra şişenin duvarlarında metalik gümüş birikmeye başlar. Bu reaksiyona gümüş ayna reaksiyonu denir. Aldehitlerin keşfinde kaliteli bir bileşik olarak kullanılır. Glikozun aldehit grubu karboksil grubuna oksitlenir. Glikoz glukonik asite dönüştürülür.
CH 2 O – (SNON) 4 – UYKU +Ag 2 Ö= CH 2 O – (SNON) 4 – COOH + 2Ag↓

İşin sırası.
İki test tüpüne 2 ml dökülür. gümüş oksitin amonyak çözeltisi. Bunlardan birine 2 ml ekleyin. % 1 glikoz çözeltisi, diğeri fruktoz. Her iki test tüpü de kaynıyor.
Gümüş oksit hidratın bir amonyak çözeltisi, gümüş nitratın sodyum hidroksit ve amonyum hidroksit ile reaksiyona sokulmasıyla elde edilir:
AgNO3+ NaOH → AgOH↓+ NaNO3,
AgOH + 2 NH4OH→[ Ag(NH3)2] OH + H2O,
amonyak çözeltisi
OH + 3 H2→ Ag2O + 4 NH4OH.
Yöntemin ilkesi. Metalik gümüşün salınması sonucu glikoz ile test tüpünün duvarlarında bir ayna oluşur.
Çalışmanın tasarımı: Sonucu, reaksiyonun gidişatını ve denklemlerini bir deftere yazın.
Deney 3. Fruktoza kalitatif reaksiyon
Yöntemin ilkesi. Fruktoz içeren bir numuneyi ortamda ısıtırken rezorsinol Ve hidroklorik asit 80 o C'ye kadar bir süre sonra fruktozlu test tüpünde parlak kırmızı bir renk belirir.
Fruktoz içeren bir numuneyi ortamda ısıtırken rezorsinol Ve hidroklorik asit kiraz kırmızısı bir renk belirir. Numune aynı zamanda diğerlerini tespit etmek için de geçerlidir. ketozis. Aldoz aynı koşullar altında daha yavaş etkileşime girerek soluk pembe bir renk verirler veya hiç etkileşime girmezler. Açık F. F. Selivanov 1887'de. İdrar analizi için kullanılır. Test, metabolik veya taşıma kaynaklı fruktozüri açısından pozitiftir. Vakaların %13'ünde meyve ve bal içeren gıdalarda test pozitif çıkar. Kimya formül fruktoz – C 6 H 12 O 6
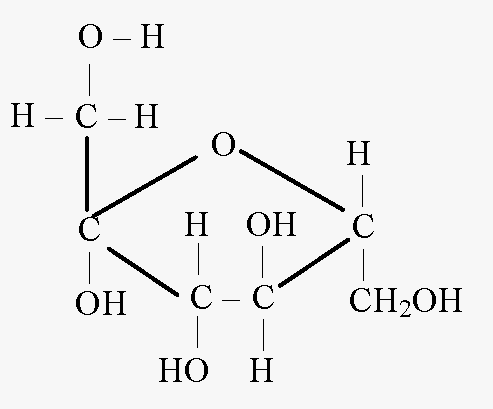
Fruktozun döngüsel formülü
Asiklik form 
fruktoz
Boyalı bağlantı
R- kalıntıları
hidroksimetilfurfural
İşin sırası.
İki test tüpüne 2 ml dökülür: birine -% 1'lik glikoz çözeltisi, diğerine -% 1'lik fruktoz çözeltisi. Her iki test tüpüne de 2 ml Selivanov reaktifi eklenir: 0,05 g resorsinol, 100 ml %20 hidroklorik asit içerisinde çözülür. Her iki test tüpü de dikkatlice 80 o C'ye ısıtılır (kaynatmadan önce). Kırmızı bir renk belirir.

Sonuçlar: Deneyin sonuçları ve reaksiyon denklemi bir deftere yazılır.